Липопротеины сыворотки крови. Классификация, состав, место образования, взаимопревращения. Роль липопротеинлипазы крови
НАВИГАЦИЯ ПО СТРАНИЦЕ
легко понять и запомнить
Для доставки эндогенных липидов другим органам и тканям в печени образуются липопротеины очень низкой плотности (ЛПОНП):
ядро – ТАГ, ЭХС;
оболочка – Апо В 100, ФЛ, ХС.
Образование ЛПОНП затрудняется при недостатке Апо В 100 и ФЛ, поэтому происходит жировое перерождение печени, в дальнейшем приводящее к циррозу.
Липотропные факторы – стимулы синтеза ФЛ:
холин;
МЕТ;
пангамовая кислота;
инозитол;
эссенциальные ВЖК;
витамины В6, В9, В12.
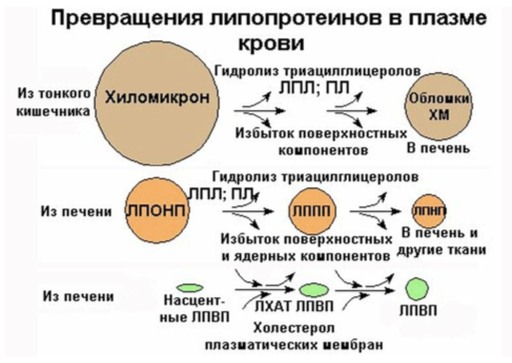
ЛПОНП выходят в кровь, где к ним приходят Апо С2 и Апо Е (от ЛПВП).
В капиллярах на ЛПОНП действует липопротеинлипаза:
ТАГ ВЖК + глицерол.
ВЖК поглощаются периферическими тканями (всеми) или как источник энергии, или для депонирования.
Поскольку ядро ЛПОНП уменьшается, его наполняют эфиры ХС, которые с помощью Апо D дают ЛПВП, и липопротеины очень низкой плотности (ЛПОНП) становятся липопротеинами промежуточной плотности (ЛППП).
75% ЛППП возвращаются в печень, захватываются рецепторами к Апо Е (R Апо Е) и уничтожаются.
25% остаются в кровотоке и подвергаются действию печеночной липазы, которая продолжает расщеплять ТАГ и забирает Апо С2 и Апо Е. В итоге, мы получили липопротеины низкой плотности (ЛПНП, самые атерогенные), в которых из всех белков остался только Апо В 100.
Печеночная липаза синтезируется в гепатоцитах, а активируется на поверхности печеночных капилляров.
75% ЛПНП с помощью рецепторов к Апо В 100 (R Апо В 100) захватывется периферическими тканями и частично печенью.
Выводы:
ЛПОНП, ЛППП, ЛПНП – транспортные формы эндогенных ТАГ и эфиров ХС из печени в периферические ткани.
Классы липопротеинов отличаются по составу, плотности и размерам:
чем больше ТАГ и меньше ядра, тем больше размер и меньше плотность.
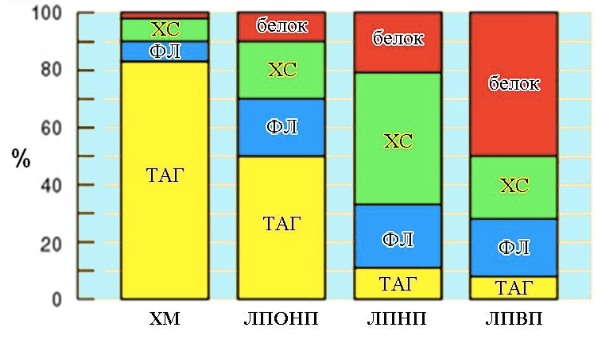
Структура липопротеинов
Работа рецепторов к Апо В 100 в периферических тканях
Апо В 100 на поверхности ЛПНП связывается с рецептором в периферической клетке, и образуется комплекс:
ЛПНП + RАпо В 100 → [ЛПНП-RАпо В 100] → эндоцитоз.
В эндосоме RАпо В 100 отщепляется и возвращается в мембрану клетки, а ЛПНП отправляется в лизосому на гидролиз:
RАпо В 100 → цитолемма;
ЛПНП → лизосома → гидролиз.
Образовавшийся в результате гидролиза своих эфиров ХС выполняет свои функции, но клетка может захватить избыток ЛПНП, отсюда избыток ХС.
Тогда включаются внутриклеточные регуляторные защитные механизмы:
активация АХАТ (Ацил-CoA-холестеролацилтрансфераза);
ингибирование ГОМГ-КоА-редуктазы;
ингибирование синтеза RАпо В 100.
Вывод:
Захват нормальных ЛПНП внепеченочными тканями не сопровождается накоплением ЭХС в клетке.
Оставшиеся 25% ЛПНП в кровотоке модифицируются:
гликозилирование;
окисление липидного компонента;
гидролиз Апо В 100 → RАпо В 100 его больше не узнают;
гидролиз ФЛ.
Атеросклероз
Такие ЛПНП – ненужный мусор, и, чтобы удалить их из кровотока, используются scavenger-макрофаги (мусорные), в которых отсутствуют механизмы самозащиты от избытка ЭХС, а R ЛПНП на них не гидролизируются → макрофаги пожирают ЛПНП в огромном количестве → превращаются в foam cells (пенистые, или ксантомные, клетки) → гибнут → выделяются цитокины → привлекаются лимфоциты → образуется аутоиммунный комплекс → пролиферация ГМК сосудов, рост соеденительной ткани → атеросклероз.
Факторы, способствующие развитию атеросклероза:
генетический дефект RАпо В 100 (семейная гиперхолестеринемия);
неблагоприятное соотношение ХС в ЛПНП и ЛПВП.
Индекс (коэффициент) атерогенности:
= = до 3
Липопротеины высокой плотности (ЛПВП)
ЛПВП помогают избавиться от избытка ХС. Они синтезируются в печени незрелыми – насцентными: много белков и ФЛ, мало гидрофобной части.
Незрелыми они выходят в кровь, приходят к клеткам органов и тканей, чтобы избавить их от избытка ХС, скопившегося на мембранах. Там его много, а в ядре ЛПВП пока еще мало, и ХС по градиенту концетрации с помощью белка АВС-1 перемещается на ЛПВП.
Но ХС сам по себе амфифилен, и с гидрофобами в ядре он находится не может, а на поверхности ЛПВП уже нет места. Выход: ХС + ЖК → гидрофобный эфир ХС.
В этом ему помогает лецитин-холестерол-ацил-трансфераза (ЛХАТ): лецитин + ХС → лизолецитин + эфир ХС.
ЛХАТ тоже синтезируется в печени и тоже в неактивном виде, Апо А1 его активирует.
Эфир ХС перемещается в ядро → ЛПВП созрел → с помощью Апо D он отдает ХМ, ЛПОНП и ЛПНП свой белковый компонент.
ЛПВП разрушается в гепатоцитах с помощью рецепторов ЛПВП и соответствующих печеночных scavenger-макрофагов. А остаток эфиров ХС попадает в желчь или в чистый ХС.
Механизм антиатерогенного действия ЛПВП:
участвуют в обратном транспорте ХС;
участвуют в утилизации липопротеинов, богатых ТАГ;
стимулируют образование простациклина;
препятствуют окислению ЛПНП;
ингибируют экспрессию адгезивных молекул на поверхности эндотелия;
уменьшают проникновение ЛПНП в интиму сосудов;
угнетают пролиферацию ГМК и уменьшают синтез ГАГ в артериальной стенке.
