Тканевое дыхание. Протонная АТФ-синтаза. Хемиоосмотическая теория окислительного фосфорилирования
НАВИГАЦИЯ ПО СТРАНИЦЕ
легко понять и запомнить
Для синтеза АТФ необходимо затратить около 32 кДж/моль энергии. Для этого достаточной является разность потенциалов между окислителем и восстановителем не менее 0,26 вольта. Чанс, Скулачев установили, что таких участков в дыхательной цепи три. Они соответствуют I, III и IV комплексам и названы пунктами сопряжения или фосфорилирования.
Чтобы понять связь между транспортом электронов по дыхательной цепи и синтезом АТФ, познакомимся с V комплексом внутренней мембраны митохондрий — ферментом, осуществляющим реакцию синтеза АТФ и называемым протонной АТФ-синтазой. Этот ферментативный комплекс состоит из двух частей: Fо (о – олигомицин), который встроен в мембрану и пронизывает ее насквозь, и F1, Последний по форме напоминает шляпку гриба или дверную ручку и обращен в матрикс митохондрии. В изолированном виде F1 не может синтезировать АТФ, но может проводить ее гидролиз до АДФ и фосфата.
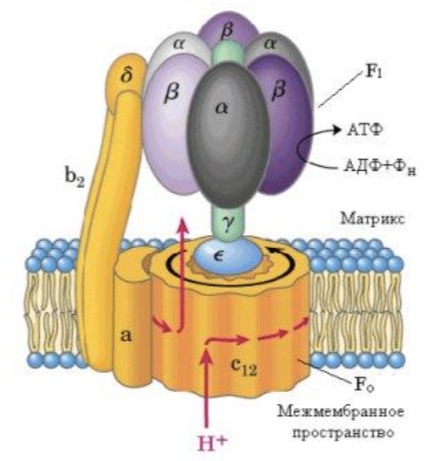
Протонная АТФ-синтаза
Реакция синтеза АТФ, которую проводит V комплекс, носит название окислительного фосфорилирования и описывается уравнением:
АДФ + Н3РО4= АТФ + Н2O
Запомнить!
В F1 идет синтез АТФ (АДФ + Фн) только тогда, когда Н+ поступают через Fo.
Если Н+ нет, то F1 работает как АТФаза, т.е. расщепляет АТФ до АДФ м Фн.
Так же синтез АТФ не идет, если отделить Fo от F1.
Биохимики долго искали связь — промежуточные макроэргические соединения, которые могли бы служить посредником между процессом тканевого дыхания и окислительным фосфорилированием. Английский биохимик П. Митчелл предположил, что синтез АТФ V комплексом ВММ сопряжен с особым состоянием этой мембраны, и сформулировал хемиоосмотическую теорию окислительного фосфорилирования (Нобелевская премия 1978 г.).
Основные постулаты этой теории:
внутренняя митохондриальная мембрана (ВММ) непроницаема для ионов, в частности для Н+ и ОН-;
за счет энергии транспорта электронов через I, III и IV комплексы дыхательной цепи из матрикса выкачиваются протоны Н+;
возникающий на мембране электрохимический потенциал (ЭХП) и есть промежуточная форма запасания энергии;
возвращение (транслокация) протонов в матрикс митохондрии через протонный канал V комплекса за счет ЭХП является движущей силой синтеза АТФ.
Механизм работы АТФ-синтазы
Дальнейшие исследования (Дж. Уокер, П. Бойер, Нобелевская премия 1997 г.) подтвердили предположения Митчелла. Ими показано, что энергия движения протонов используется на изменения конформации активного центра АТФ-синтазы, что сопровождается синтезом АТФ, а затем ее высвобождением. Образовавшаяся АТФ с помощью транслоказы перемещается в цитозоль; в ответ в матрикс митохондрии поступают АДФ и фосфат. Всего на процесс синтеза, высвобождения и выброса в цитозоль расходуется 4 протона.
При окислении НАД-зависимых субстратов в ММП выбрасывается 10 протонов. Следовательно, в таком случае может быть синтезировано 2,5 моль АТФ (10:4), т.е. коэффициент фосфорилирования Р/О = 2,5.
При окислении ФАД-зависимых субстратов в ММП выбрасывается 6 протонов в III и IV пунктах сопряжения. В таком случае может быть синтезировано 1,5 моль АТФ (6:4), т.е. коэффициент фосфорилирования Р/О = 1,5.
Регулируется скорость работы дыхательной цепи энергетическим зарядом клетки, т. е. соотношением АТФ/АДФ. АДФ является стимулятором дыхательной цепи, АТФ – аллостерическим ингибитором.
Гипоэнергетические состояния возникают в организме вследствие дефицита АТФ в клетках. Причины их следующие:
алиментарные (голодание, гиповитаминозы РР, В2);
гипоксические (нарушения доставки О2 в клетки);
митохондриальные (действие ингибиторов и разобщителей).
