Химические реакции
НАВИГАЦИЯ ПО СТРАНИЦЕ
легко понять и запомнить
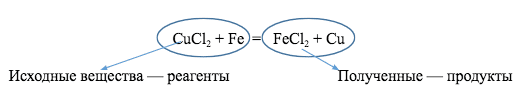
В результате химических превращений масса веществ остается неизменной — общая масса всех исходных веществ равна общей массе всех продуктов реакции. Это
Равенство масс исходных веществ и продуктов реакции объясняется тем, что в процессе протекания химических реакций новые вещества образуются из тех же атомов, из которых состояли реагенты. Не образовываются новые атомы, не исчезают старые и не происходит превращения одних атомов в другие. Атомы перегруппировываются.
Для записи химических реакций используют
Схема химической реакции показывает только реагенты и продукты, но обычно в нее не записывают коэффициенты.
Например:
— схема;
— уравнение.
Уравнение реакции отражают, какие вещества и в каком отношении вступили и образовались в ходе реакции. Для записи реагентов и продуктов реакции используют химические формулы веществ, для указания отношения, в котором вещества реагируют и образуются, используют численные коэффициенты. При этом
Рассмотрим это на примере взаимодействия оксида алюминия и оксида углерода (II), для начала запишем реагенты:
В ходе данной реакции образуется цинк и углекислый газ, запишем их формулы после стрелки:
В левой части уравнения 2 атома алюминия, а в правой — один, значит, необходимо удвоить количество атомов алюминия справа:
Атомов кислорода слева 4, а справа 2, казалось бы, что мы можем поставить 2 перед формулой угарного газа и все уравняется:
Но, теперь у нас разное количество атомов углерода, перед атомами углерода должны быть одинаковые коэффициенты, поэтому 2 перед СО нам не подходит:
Можем поставить тройки перед газами и получить равное количество углерода и кислорода в обеих частях уравнения:
Теперь, наконец, количество атомов всех элементов в правой и левой частях уравнения химической реакции равно, на этом запись уравнения реакции закончена.
