Окислительно-восстановительные реакции. Понятия окислитель и восстановитель
НАВИГАЦИЯ ПО СТРАНИЦЕ
легко понять и запомнить
Окислительно-восстановительные реакции (
Окислительно-восстановительная реакция складывается из двух процессов: процесса окисления и процесса восстановления.
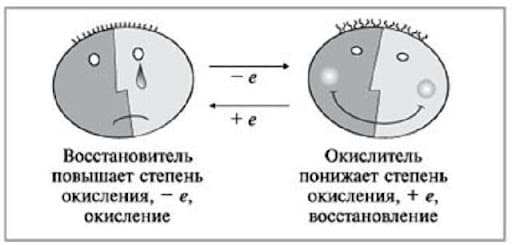
Такой атом называют атомом-восстановителем, вещество, в состав которого входит этот атом, также называют
Такой атом называют атомом-окислителем, вещество, в состав которого входит этот атом, также называют окислителем.
Для успешного составления уравнений ОВР в первую очередь необходимо научиться понимать, какие из веществ в принципе могут проявлять окислительные, а какие — восстановительные свойства, а также насколько сильно выражены эти свойства.
Что касается силы окислителей и восстановителей, подробное количественное рассмотрение этого аспекта ОВР выходит за рамки школьной программы, однако на качественном уровне этот вопрос будет освещаться на этом и дальнейших занятиях, посвященных химии элементов.
Одним из основных факторов, определяющих окислительно-восстановительные свойства соединений, являются
Элементы в низших степенях окисления могут быть
Окислительно-восстановительной двойственностью, как можно догадаться, обладают соединения, в составе которых имеются элементы в промежуточных степенях окисления. И окислителями, и восстановителями могут выступать простые вещества-неметаллы, соединения , , и т. д.
Если речь идет о кислородсодержащих ионов вида , то их окислительно-восстановительные свойства определяются центральным атомом. Несмотря на то, что в их состав входит кислород в низшей степени окисления, его восстановительные свойства могут проявляться в очень ограниченном числе реакций, поэтому их обычно выбрасывают из рассмотрения.
Мы уже сталкивались с ОВР, например, при взаимодействии растворов щелочей, кислот и солей с металлами. Однако различных ОВР множество, и при рассмотрении химических свойств различных веществ их окислительно-восстановительные свойства ничуть не менее важны, чем кислотно-основные.
Определение продуктов реакций и расстановка коэффициентов в уравнениях ОВР может вызывать определенные трудности. Для грамотного предсказания продуктов ОВР необходимо обладать багажом знаний по химии элементов, знать, какие степени окисления могут проявлять элементы, какие формы существования соответствуют этим степеням окисления в различных средах и как соотносятся окислительная и восстановительная способности участников реакции.
Для расстановки коэффициентов в уравнениях ОВР существует несколько методов, которые основываются на том, что количество электронов, отдаваемых восстановителем, должно быть равно количеству электронов, принимаемых окислителем.
