Углерод. Электронное строение, основные аллотропные модификации, способы получения
НАВИГАЦИЯ ПО СТРАНИЦЕ
легко понять и запомнить
Углерод – неметалл, элемент с порядковым номером 6, расположен в 2 периоде IVA группе Периодической системы химических элементов Д.И. Менделеева.
Электронное строение атома углерода
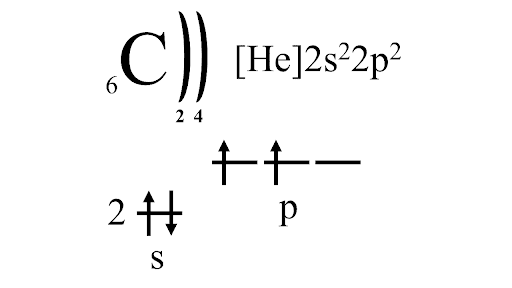
Возможные степени окисления: -4, 0, +2, +4. В органических соединениях могут проявляться все возможные степени окисления от -4 до +3.
Валентность в соединениях: III, IV.
Простое вещество углерод
Углерод имеет самое большое количество аллотропных модификаций, наиболее важные их них: алмаз, графит и аморфный углерод. Кроме того, углерод может существовать в форме графена, фуллеренов, углеродных нанотрубок и др.

Алмаз представляет собой чрезвычайно твердое и химически инертное вещество. Имеет атомную кристаллическую решетку. Не растворяется в воде или органических жидкостях.
Графит представляет собой мягкое твердое вещество со слоистой структурой, проводящее электрический ток. Имеет атомную кристаллическую решетку. Не растворяется в воде или органических жидкостях.
Аморфный углерод – общее название для различных форм существования углерода, общим для которых является отсутствие четко выраженной структуры. Не растворяется в воде или органических жидкостях.
Способы получения углерода
Некоторые аллотропные модификации угля, например, алмаз и графит встречаются в природе. Другие, например фуллеренов, необходимы в ограниченных количествах, а их получение достаточно трудоемкая процедура. Так что в рамках разговора о способах получения угля целесообразно остановится подробно лишь на получении кокса.
Кокс – продукт коксования природных углей или нефтей. Коксование представляет собой процесс переработки твердого или жидкого природного топлива, заключающийся в его длительном нагревании без доступах воздуха.
В ходе коксования угли и нефти теряют заключенные в них сопутствующие вещества, а также подвергаются разложению. Побочными продуктами коксования являются улетучивающиеся вода, углекислый и угарный газ, легкие углеводороды, аммиак и другие соединения азота, соединения фосфора, сероводород и водород. Образующийся кокс содержит до 98% углерода и используется в качестве топлива и восстановителя в металлургии.
